
时间:2024-02-20 访问量:643 来源:管理员
不要把做笔记当做任务,而是当做思考、总结、归纳的过程,通过思考可以更熟悉知识点,便于记忆,才能更好发挥它的作用。盛世清北十年来专注清北硕博辅导,为帮助考生少走弯路,整理如下清华深研院材料与化工(专业学位)考研相关资料,以供参考。
参考书(仅供参考,可能会随年份变化,可咨询盛世清北老师)
975材料物理化学:
《材料科学基础》2011 年修订版,潘金生、仝健民、田民波著,清华大学出版社。
《无机材料物理性能》第 2 版,关振铎、张中太、焦金生著,清华大学出版社。
《简明物理化学》2008 年版,朱文涛,王军民,陈琳著,清华大学出版社。
837物理化学:
《材料科学基础》清华大学出版社,潘金生,仝建民,田民波
《物理化学》清华大学出版社,朱文涛
《物理化学》高等教育出版社,傅献彩等
考情分析
真题解读:
经近几年的历年真题分析,盛世清北老师得出如下结论:
专业课 | 题型 | 分值 | 备注 |
975 材料物理化学 | 基本概念题(单选、多选、填空、判断、名词解释等) | 66 分 | 总分150分,考试时间180分钟 |
问答题(简答、分析论述等) | 39分 | ||
计算分析题 | 45分 | ||
837 物理化学 | 选择题 | 70分 | 总分150分,考试时间180分钟 |
分析题 | 40分 | ||
计算题 | 40分 |
解读
1、材料与化工专业课历年考试难度大,考题较为灵活,与社会热点关联更深。同时,也关注考生的知识面。
2、报考清华也需要有扎实的基础,并非通过所谓的押题和划重点就能考上的。
历年分数线
年份 | 政治 | 外语 | 专业课一 | 专业课二 | 总分 | 拟录取人数 | 复试最高分/最低分 | 方向 |
2023 | 50 | 50 | 80 | 70 | 325 | 55 | 395/326 | 功能与器件 |
7 | 390/329 | 健康工程 | ||||||
21 | 428/325 | 制药工程 | ||||||
2022 | 50 | 50 | 80 | 70 | 325 | 49 | 393/326 | 功能与器件 |
21 | 428/325 | 制药工程 | ||||||
2021 | 50 | 50 | 80 | 70 | 310 | 51 | 416/314 | 功能与器件 |
15 | 392/317 | 制药工程 | ||||||
2020 | 50 | 50 | 70 | 70 | 300 | 57 | 425/300 | 功能与器件 |
45 | 45 | 70 | 70 | 300 | 11 | 390/326 | 制药工程 |
解读:
根据近4年分数线及复试情况,盛世清北老师分析如下:
(1)近四年来,各科目分数线趋于平稳状态,而总分数线存在波动,且2022年和2023年分数线最高,意味着难度逐步增加,应更加重视专业课的复习,要早复习,避免走弯路。
(2)四年中,健康工程录取最低分329分,最高分390分,制药工程录取最低分是317分,最高分是428分,功能与器件录取最低分是300,最高分是425,也就是说我们努力考分在300-428之间很有机会进入材料与化工复试。
(3)制药工程录取人数2020年是11人,2021年是15人,2022年15人,2023年21人,说明招生人数有扩招的可能性;功能与器件录取人数2020年是57人,2021年是51人,2022年49人,2023年55人,说明招生人数有扩招的可能性,同学们要抓住这个机会。
(4)材料与化工(专业学位)的复试录取比例较大,复试会淘汰一部分,要非常重视复试;
975 材料物理化学考试大纲(2022 年 6 月修订)
一、 考核内容
1、 材料学基础
1.1、晶体学基础
布拉维点阵;晶体结构;典型金属晶体中的间隙;晶面指数与晶向指数;标准投影;晶体的堆垛方式。
1.2、固体材料的结构
元素的晶体结构;合金相结构;固溶体;离子化合物。
1.3、晶体中的缺陷
点缺陷(概念、种类、平衡浓度);位错(概念、运动、受力、交互作用、反应);界面的定义与分类;晶界模型;界面能;界面偏聚。
1.4 材料热力学与相图
热力学基本概念;单组元、合金体系和多相体系的热力学关系;自由能构建相图与相律;相图的基本概念;二元和三元相图;利用相图分析相和组
织等;相图与性能关系。
1.5、固体中的扩散
扩散的概念与分类;Fick 定律;稳态和非稳态扩散;Kirkendall 效应;扩散的微观机制;影响扩散的因素;反应扩散;扩散的应用。
2、 材料物理
2.1 材料的电导与介电性能
电导的基本概念;电子电导;离子电导;介质的极化;介质的损耗;介电强度;铁电/压电性。
2.2 材料的热学性能
固体的热容;材料的热膨胀;材料的热导率;材料的热稳定性。
3、 材料化学
3.1 化学平衡
化学反应的方向和限度;化学反应的标准摩尔 Gibbs 函数变化;平衡常数及各种因素的影响。
3.2 电化学平衡
库仑定律;电场和电势;电解质的导电机理与 Faraday 定律;可逆电池及可逆电极;可逆电池电动势;可逆电极电势;浓差电池。
3.3 表面化学与胶体的基本知识
表面能和表面张力的基本概念;弯曲表面下的附加压力—Young-Laplace 方程;固-液界面;溶液表面;固体表面的吸附。
3.4 化学动力学基础
化学反应速率;物质浓度、温度、活化能对反应速率的影响;具有简单级数的化学反应;反应级数的测定;催化剂对反应速率的影响;均相和多相催化。
837《物理化学》考试大纲
一、考试性质
837《物理化学》是清华大学深圳国际研究生院材料与化工大类制药工程、健康工
程方向的统考考试科目。本专业课考试科目力求科学、公平、准确、规范地考察学生对
专业基础知识的综合理解和运用。
二、考试范围
1 热力学常见基本概念
1.1 系统、环境与边界
1.2 强度性质与广度性质
1.3 状态与平衡状态
1.4 过程与途径
1.5 热平衡与热力学第 0 定律
1.6 温度与热力学温度
2 气体
2.1 理想气体
2.2 状态方程
2.3 实际气体
2.3.1 压缩因子
2.3.2 维里方程
2.3.3 范德华方程
3 热力学第一定律
3.1 热量与功
3.2 热功等效与内能
3.3 热力学第一定律(能量守恒定律)
3.4 功与体积功
3.4.1 体积功的计算
3.4.2 不可逆与可逆过程
3.5 热与热容
3.5.1 等容热效应
3.5.2 等压热效应与焓
3.5.3 热容及简单变温过程热的计算
3.6 热力学第一定律在气体中的应用
3.6.1 内能和焓的计算通式
3.6.2 节流过程与 Joule-Thomson 系数
3.6.3 理想气体和范德华气体的内能与焓计算
3.6.4 等温、绝热、等容过程方程
3.6.5 热力学循环
3.7 第一定律对于化学反应的应用——热化学
3.7.1 化学反应进度
3.7.2 化学反应的热效应
3.7.3 反应热的计算
3.7.4 反应热的测量
3.7.5 反应热与温度的关系
3.7.6 非等温反应系统
4 热力学第二定律
4.1 自发过程的共同特征
4.1.1 自发过程的方向和限度
4.1.2 自发过程的共同特征
4.2 热力学第二定律的表述和过程的方向性
4.2.1 热力学第二定律的表述
4.2.2 过程方向和限度的描述方法
4.3 Carnot 循环和 Carnot 定理
4.3.1 Carnot 循环的效率
4.3.2 Carnot 定理及其推论
4.4 熵与混乱度
4.4.1 熵的导出
4.4.2 热力学第二定律的数学表达式—Clausius 不等式
4.5 熵判据
4.5.1 熵增加原理
4.5.2 熵的物理意义
4.6 熵变的计算
4.6.1 简单物理过程的熵变
4.6.2 相变过程的熵变
4.6.3 混合过程的熵变
4.6.4 环境熵变
4.7 热力学第三定律和规定熵
4.7.1 Nernst 热定理
4.7.2 热力学第三定律
4.7.3 规定熵的计算
4.7.4 化学反应的熵变
5 热力学基本关系式与热力学函数
5.1 内能与熵
5.2 勒让德变换与热力学函数
5.3 平衡与稳定判据
5.3.1 Helmholtz 函数及 Helmholtz 函数减少原理
5.3.2 Gibbs 函数及 Gibbs 函数减少原理
5.3.3 关于判据的总结
5.4 各个热力学函数间关系
5.4.1 Gibbs 公式
5.4.2 对应系数关系式
5.4.3 Maxwell 关系式
5.4.4 基本关系式的应用
5.5 ∆G 及∆A 的计算
5.5.1 简单物理变化过程的∆G 和∆A
5.5.2 相变过程的∆G 和∆A
5.5.3 混合过程的∆G
5.5.4 ∆G 随 T 的变化
6 溶液热力学
6.1 溶液的特点及组成表示法
6.1.1 溶液的特点
6.1.2 溶液组成的习惯表示方法
6.2 偏摩尔量
6.2.1 质点数目可变系统的状态描述
6.2.2 偏摩尔量
6.2.3 偏摩尔集合公式
6.2.4 Gibbs-Duhem 公式
6.2.5 偏摩尔量的测量
6.3 化学势
6.3.1 化学势的定义
6.3.2 敞开系统的基本关系式和化学势的其他形式
6.3.3 化学势决定传质过程的方向和限度
6.3.4 化学势与 T 和 p 的关系
6.4 气体的化学势
6.4.1 理想气体的化学势
6.4.2 化学势的统计推导方法
6.4.3 实际气体的化学势
6.4.4 气体的逸度和逸度系数
6.4.5 气体热力学函数的非理想性修正
6.5 Raoult 定律和理想溶液
6.5.1 Raoult 定律
6.5.2 理想溶液及其化学势
6.5.3 理想溶液的通性
6.6 Henry 定律和理想稀薄溶液
6.6.1 Henry 定律
6.6.2 理想稀薄溶液及其化学势
6.6.3 依数性
6.6.4 二元溶液中溶剂和溶质性质的相关性
6.7 非理想溶液
6.7.1 活度和活度系数
6.7.2 非理想溶液的化学势
6.7.3 关于化学势、标准态和活度的总结
6.7.4 非理想溶液的混合性质和依数性
6.7.5 活度的测定与计算
6.7.6 超额热力学函数
6.8 分配定律
7 相平衡
7.1 相平衡的必要条件
7.1.1 相和相数的确定
7.1.2 相平衡的必要条件
7.2 相律
7.2.1 系统的物种数和组分数
7.2.2 自由度和自由度数
7.2.3 相律
7.3 单组分系统的两相平衡
7.3.1 Clapeyron 方程
7.3.2 压力对蒸气压的影响
7.4 单组分系统的相图
7.4.1 水的相图
7.4.2 硫的相图
7.5 二组分理想溶液的气-液相图及其应用
7.5.1 p-x 图(蒸气压-组成图)
7.5.2 T-x 图(沸点-组成图)
7.5.3 杠杆规则——质量守恒的必然结果
7.5.4 分馏原理
7.6 二元组分非理想溶液的气-液相图
7.6.1 偏差不大
7.6.2 偏差很大
7.7 部分互溶双液系的液-液相图
7.8 完全不互溶的双液系统
7.9 二组分系统的固-液相图
7.9.1 具有简单低共熔混合物的相图
7.9.2 具有稳定化合物的相图
7.9.3 具有不稳定化合物的相图
7.9.4 形成固溶体的相图
7.10 依数性原理
7.11 相图的规律性
7.11.1 二组分系统相图的总结
7.11.2 相图的结构
8 化学平衡
8.1 化学反应的方向和限度
8.1.1 非平衡系统的热力学性质
8.1.2 化学平衡的条件
8.1.3 平衡常数的导出
8.1.4 化学反应方向的判断
8.2 化学反应的标准摩尔 Gibbs 函数变
8.2.1 ∆rG![]() 的意义
的意义
8.2.2 ∆rG![]() 的计算
的计算
8.2.3 ∆rG![]() 与 T 的近似线性关系及其应用
与 T 的近似线性关系及其应用
8.3 关于平衡常数的讨论
8.3.1 平衡常数的意义
8.3.2 影响平衡常数的因素
8.3.3 平衡常数的具体形式
8.3.4 求算平衡常数的基本方法
8.4 平衡计算举例
8.4.1 计算平衡常数
8.4.2 计算平衡组成
8.5 各种因素对于化学平衡的影响
8.5.1 平衡移动问题的共性
8.5.2 温度对于化学平衡的影响
8.5.3 压力对于化学平衡的影响
8.5.4 惰性气体对于化学平衡的影响
8.5.5 浓度对于化学平衡的影响
9 电化学平衡
9.1 库仑定律、电场和电势
9.2 电解质溶液的导电机理与 Faraday 定律
9.3 可逆电池及可逆电极的一般知识
9.4 可逆电池电动势的测量与计算
9.5 可逆电极电势
9.6 浓差电池及液接电势
9.7 电动势法的应用
10 表面化学与胶体的基本知识
10.1 基本概念
10.1.1 表面功和表面能
10.1.2 表面张力
10.1.3 影响表面张力的主要因素
10.2 弯曲表面下的附加压力——Young-Laplace 方程
10.2.1 Young-Laplace 方程的应用
10.2.2 弯曲表面下液体的蒸气压——Kelvin 方程
10.2.3 固体颗粒大小对于溶解度的影响
10.2.4 固体熔点与颗粒半径的关系
10.3 固-液界面
10.3.1 液体对固体的润湿作用
10.3.2 液体在固体表面上的铺展
10.3.3 毛细现象及表面张力的测定方法
10.4 溶液表面
10.4.1 溶液的表面张力与表面吸附现象
10.4.2 Gibbs 吸附方程
10.5 固体表面
10.5.1 固体表面对气体的吸附现象
10.5.2 Langmuir 吸附理论
10.5.3 BET 吸附理论
10.5.4 Freundlich 公式
10.5.5 吸附热力学
10.5.6 吸附的本质——物理吸附和化学吸附
11 化学动力学基础
11.1 基本概念
11.1.1 化学反应速率
11.1.2 元反应及反应分子数
11.1.3 简单反应和复合反应
11.2 物质浓度对反应速率的影响
11.2.1 速率方程
11.2.2 元反应的速率方程——质量作用定律
11.2.3 反应级数与速率系数
11.3 具有简单级数的化学反应
11.3.1 一级反应
11.3.2 二级反应
11.3.3 三级反应和零级反应
11.4 反应级数的测定
11.4.1 几点说明
11.4.2 r=![]() 型反应级数的测定
型反应级数的测定
11.4.3 r=![]() C
C![]() …型反应级数的测定
…型反应级数的测定
11.5 温度对反应速率的影响
11.5.1 经验规则
11.5.2 Arrhenius 公式
11.6 活化能及其对反应速率的影响
11.6.1 元反应的活化能
11.6.2 微观可逆原理及其推论
11.6.3 复合反应的活化能
11.6.4 活化能对反应速率的影响
11.6.5 Arrhenius 公式的修正
11.6.6 活化能的求取
11.7 元反应速率理论
11.7.1 碰撞理论
11.7.2 势能面和反应坐标简介
11.7.3 过渡状态理论
11.7.4 两个速率理论与 Arrhenius 公式的比较
11.8 反应机理
11.8.1 对峙反应
11.8.2 平行反应
11.8.3 连续反应
11.8.4 链反应
11.8.5 稳态假设与平衡假设
11.8.6 反应机理的推测
11.8.7 微观反应动力学简介
11.9 催化剂对反应速率的影响
11.9.1 催化剂和催化作用
11.9.2 催化机理
11.9.3 催化剂的一般性质
11.10 均相催化反应和酶催化反应
11.10.1 均相催化反应
11.10.2 酶催化反应
11.11 多相催化反应
11.11.1 催化剂的活性与中毒
11.11.2 催化剂表面活性中心的概念
11.11.3 气-固两相催化反应的一般步骤
11.11.4 催化作用与吸附的关系
真题试题
2020年清华大学975材料物理化学考研试题



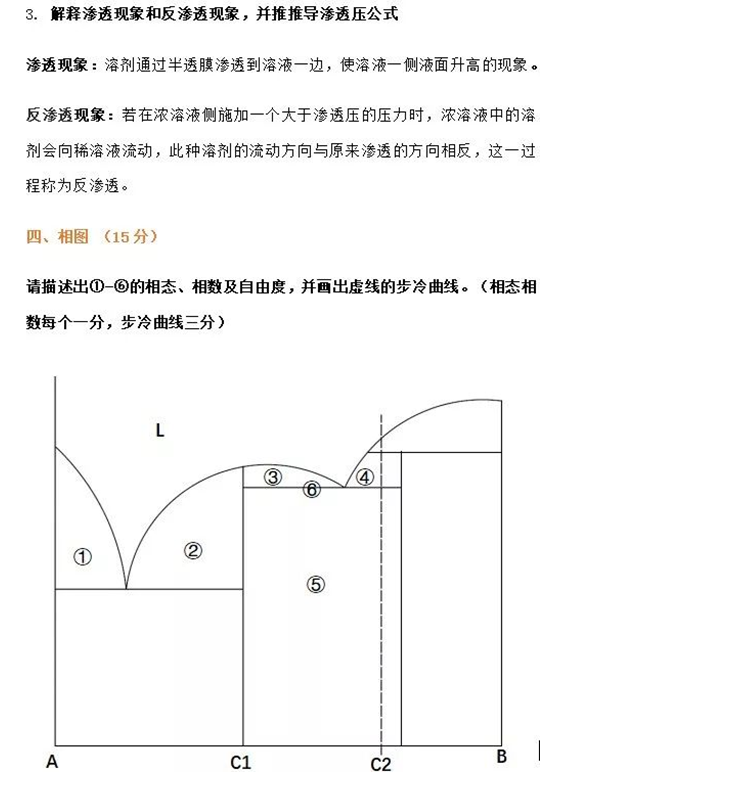



生活是公平的,哪怕吃了很多苦,只要你坚持下去,一定会有收获,即使最后失败了,你也获得了别人不具备的经历。加油,考研人!
以上就是盛世清北小编整理的“清华深研院材料与化工(专业学位)考研干货笔记”相关内容,更多清华大学研究生招生考试相关内容尽在盛世清北-清华考研栏目!愿你考研路上一帆风顺!